Yeni BioNTech aşısı sonbaharda piyasaya çıkacak
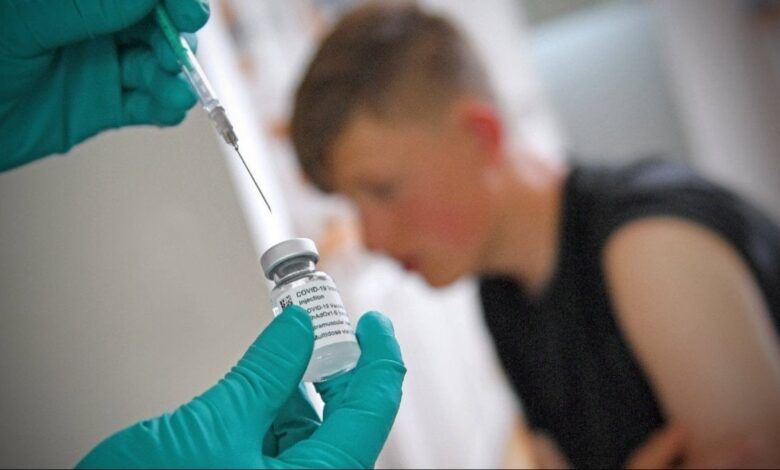
Corona virüsünün alt varyantlarına karşı tesirli olacak aşıların sonbaharda hazır olması bekleniyor.
Deutsche Welle Türkçe’nin Alman Hekimler Gazetesi’ne dayandırdığı habere nazaran Alman biyoteknoloji firması BioNTech, alt varyantlara karşı tesirli olacak aşısını resmi onaylara bağlı olarak Avrupa’da Eylül ayında teslim etmeyi planladığını açıkladı.
BioNTech ve ABD’li Pfizer şirketinin, Omicron varyantının alt varyantı XXB.1,5’ye karşı aşı geliştirdiği açıklandı. Almanya ve Avrupa’nın birçok ülkesinde giderek yayılan yeni varyant EG.5’in de XBB’den türediği belirtiliyor.
ABD’li Moderna firması da gazeteye yaptığı açıklamada, geliştirdiği aşının sonbahara yetişeceği iletisini verdi ve onay almasının akabinde piyasaya sürüleceğini kaydetti. Bunun yanı sıra ABD’li Novavax firması da tıpkı formda Omicron’un alt varyantına karşı tesirli olacak bir aşı üzerinde çalışıyor.
Gazeteye nazaran yeni aşıların kullanımının daha kolay olması planlanıyor. Biyoteknoloji şirketleri öncelikle aşıları tek dozluk formda üretecek. Daha öncesinde aşılar birkaç dozluk olarak üretiliyor ve açılmaları halinde kısa müddet içinde kullanılmaları gerekiyordu.
UĞUR ŞAHİN’DEN TEPKİ
BioNTech’in kurucusu Uğur Şahin Frankfurter Allgemeine Zeitung’a yaptığı açıklamada, yeni ilaçlar geliştirilirken onay sürecindeki verimsiz ve uzun prosedürü eleştirdi.
İlk aşı geliştirilirken yetkili ünitelerle yapılan ağır işbirliğine dikkat çeken Şahin, “Şimdi yine olağana döndük ve bu tekrar uzun bir süreç süreci manasına geliyor. Almanya ve Avrupa’da çok uzman düzenleyici üniteler var. Lakin hem yetkili makamlar, hem de ilaç geliştiricilerinin kaynaklarını büyük oranda tüketen verimsiz bir süreç var” diye konuştu.
Şahin, teknolojik imkanlarla bürokrasinin müsaade verdikleri ortasında bir uyumsuzluk olduğunu söyleyerek “Bunun nedeni gereksiz bürokrasi. Bir öteki eksiklikse süreç müddetlerini uzatan kaynak eksikliği” dedi. Şahin ilacın çok değerli olduğunu belirterek, “Sistemin tembelliği onayları geciktiren bir darboğaz olmamalı” tabirini kullandı.
Avrupa Birliği’nde (AB) ilaç ya da aşıların onay alma süreci birkaç etaptan oluşuyor. Bu evreler ortasında çok sayıda klinik araştırmasının yapılması şartı da bulunuyor. Bu basamakların sonucunda Avrupa İlaç Ajansı (EMA) kelam konusu ilaç ya da aşıya dair görüşünü açıklıyor ve Avrupa Birliği Kurulu da onay konusunda kararını açıklıyor. AB Komitesi gelecekte onay sürecindeki son iki etap için belirlenen müddetin kısaltılabileceğini duyurmuştu.











